DNAローディング色素は、アガロースまたはポリアクリルアミドゲル中でDNAの移動を追跡するために使用されます。
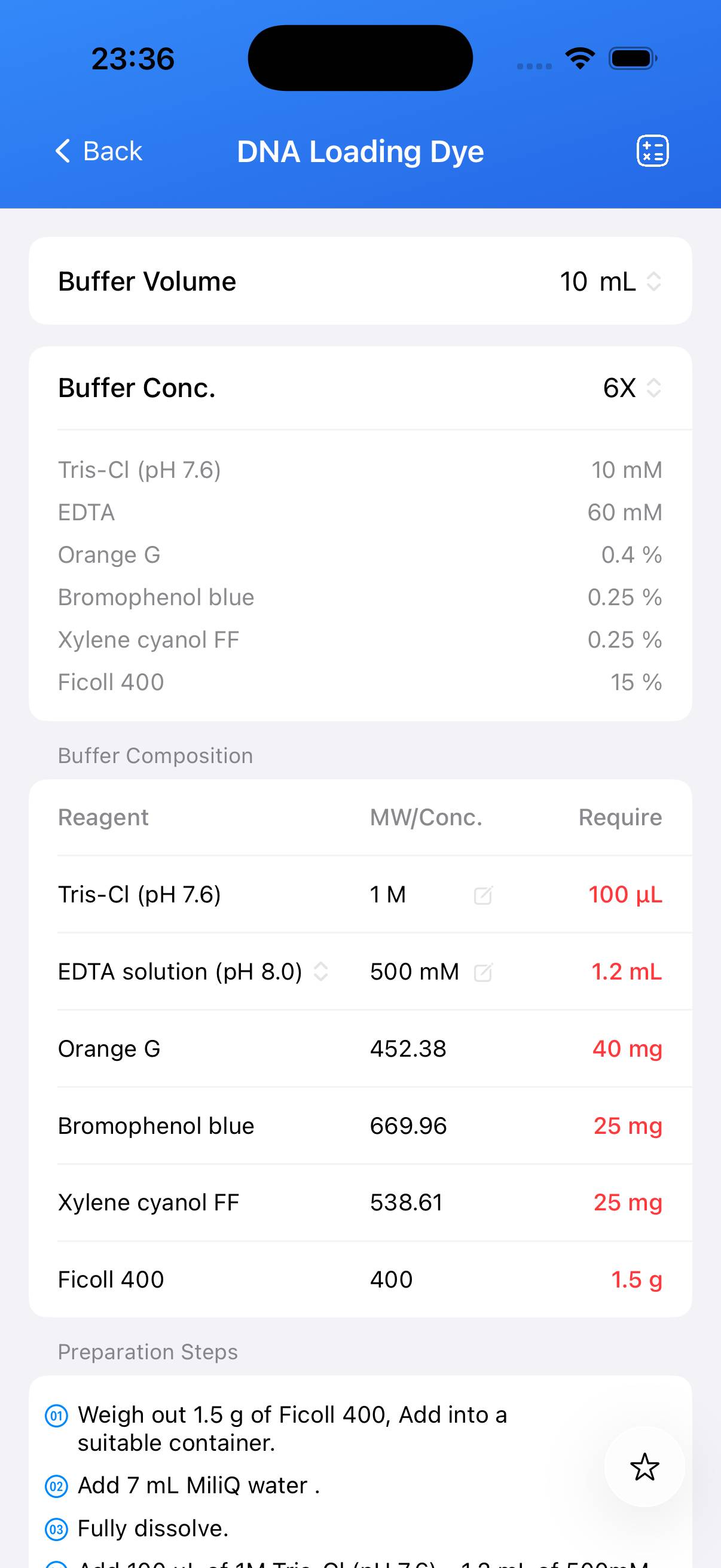
6X DNAローディング色素 — 組成
| 名称 | 化学式 | 濃度 | CAS |
|---|---|---|---|
| Tris-Cl (pH 7.6) | C₄H₁₁NO₃ | 10 mM | 77-86-1 |
| EDTA | C₁₀H₁₆N₂O₈ | 60 mM | 60-00-4 |
| Orange G | C₁₆H₁₀N₂Na₂O₇S₂ | 0.4% (w/v) | 1936-15-8 |
| Bromophenol blue | C₁₉H₁₀Br₄O₅S | 0.25% (w/v) | 115-39-9 |
| Xylene cyanol FF | C₂₅H₂₇N₂NaO₆S₂ | 0.25% (w/v) | 2650-17-1 |
| Ficoll 400 | (C₁₂H₂₂O₁₁)n·(C₃H₅ClO)n | 15% (w/v) | 26873-85-8 |
滅菌と保存
- 滅菌:不要。
- 保存:1 mLチューブに分注し、4°Cまたは−20°C。
ポイント
- DNAローディング色素には多くの処方があり、ここでは一例のみ示しています。
- 色素(ステップ4まで)を添加する前は、溶液が無色〜黄みがかった濁りに見える場合があります。
- 少量(例:10 mL)を調製する際は、容量調整前にチューブ壁やキャップに残液がないことを確認してください。
- 溶液は粘性が高くピペッティングしにくいため、可能なら適切な容器1つで完結させてください。
- 色素濃度は調整可能です:ブロモフェノールブルー/キシレンシアノールFF 0.03%〜0.50%(w/v)、Orange G 0.15%〜0.50%(w/v)。
- 高濃度は視認性を高めますが、共移動するDNAバンドを見えにくくする場合があります。共移動が予想される場合は低濃度を使用してください。
- Ficoll 400は60%(v/v)グリセロールまたは40%(w/v)スクロースで代替可能です。スクロース溶液は凍結保存してください。
- Ficollを含むローディング色素はDNAをアガロース中に沈みやすくしますが、コストが高くなります。
- 三色のローディング色素はDNA断片の分離状態をより分かりやすく示しますが、価格は高めです。
Preview